
Sadržaj
Atomi su premali da bi mogli dopustiti bilo kakvo značajno mjerenje kemikalija. Da bi radili sa značajnim količinama ovih tvari, znanstvenici ih grupiraju u jedinice koje se nazivaju madeži. Mol se definira kao broj atoma ugljika u 12 g izotopa ugljik-12, što je oko 6,022 x 10 atoma. Taj se broj naziva Avogadrovim brojem ili konstantom. Koristi se za određivanje broja atoma bilo koje tvari. Uz to, masa jednog mola tvari je molarna masa.
Koraci
Metoda 1 od 2: Izračunavanje molarne mase elementa
Pokušajte razumjeti molarnu masu. To je masa (u gramima) mola tvari. Koristeći atomsku masu elementa i pomnoživši je s faktorom pretvorbe u gramima po molu (g / mol), moguće je izračunati molarnu masu tog elementa.
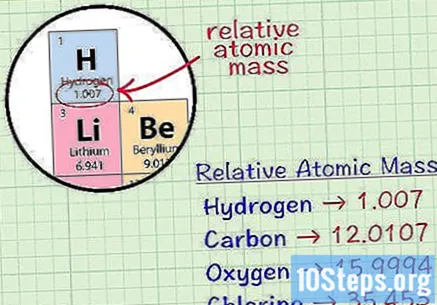
Pronađite relativnu atomsku masu elementa. To je prosječna masa, u atomskim jedinicama, uzorka svih izotopa elementa. Te se informacije mogu naći u periodnom sustavu elemenata. Jednostavno locirajte element i broj će biti ispod njegovog simbola. Uz to, ovaj broj neće biti cijeli broj, već decimalni znak.- Na primjer, za vodik je relativna atomska masa 1,007; za ugljik je 12,0107; za kisik je 15,9994; a za klor je 35.453.

Pomnožite relativnu atomsku masu s konstantom molarne mase. Definira se kao 0,001 kg po molu ili 1 g po molu. To je pretvorba atomskih jedinica u grame po molu, čineći molarnu masu vodika 1,007 g / mol, masu ugljika 12,0107 g / mol, kisika 15,9994 g / mol i klora 35,453 g / mol.- Neki se elementi nalaze u molekulama sa samo dva ili više atoma. To znači da je za pronalaženje molarne mase elemenata sastavljenih od dva atoma, poput vodika, kisika i klora, potrebno pronaći njihove relativne atomske mase, pomnožiti ih s konstantom molarne mase, a zatim pomnožiti rezultat za dvoje.
- Za H2: 1.007 x 2 = 2.014 g / mol; za2: 15,9994 x 2 = 31,9988 g / mol; a za Cl2: 35,453 x 2 = 70,096 g / mol.
Metoda 2 od 2: Izračunavanje molarne mase spoja

Pronađite kemijsku formulu spoja. Sastoji se od broja atoma u svakom elementu koji čini spoj (ove informacije mogu se dobiti iz bilo kojeg priručnika iz kemije). Na primjer, formula za klorovodik (klorovodičnu kiselinu) je HCl, a formula glukoze je C6H12THE6. Pomoću ove formule moguće je identificirati broj atoma svakog elementa koji čini spoj.- HCl ima atom vodika i atom klora.
- C6H12THE6 ima šest atoma ugljika, 12 atoma vodika i šest kisika.
Pronađite relativnu atomsku masu svakog elementa spoja. Pomoću periodnog sustava pronađite relativnu atomsku masu svakog elementa (broj koji se nalazi ispod simbola elementa). Na isti način kao i izračun molarne mase elementa u prvom koraku, te će se mase također pomnožiti s 1 g / mol.
- Relativne atomske mase elemenata koji čine solnu kiselinu su: 1,007 g / mol vodika i 35,453 g / mol klora.
- Relativne atomske mase elemenata koji čine glukozu su: 12,0107 g / mol ugljika, 1,007 g / mol vodika i 15,9994 g / mol kisika.
Izračunajte molarnu masu svakog elementa spoja. Pomnožite atomsku masu elementa s brojem atoma u spoju. To će rezultirati relativnom količinom koju svaki element doprinosi spoju.
- Molarna masa svakog elementa klorovodične kiseline (HCl) iznosi: 1,007 g / mol vodika i 35,453 g / mol klora.
- Molarna masa svakog elementa glukoze (C6H12THE6) je: 12,0107 x 6 = 72,0642 g / mol ugljika, 1,007 x 12 = 12,084 g / mol vodika i 15,9994 x 6 = 95,9964 g / mol kisika.
Dodajte molarne mase svakog elementa u spoju. Učinite to da odredite ukupnu molarnu masu spoja. Uzmite proizvode dobivene u prethodnom koraku i zbrojite ih sve da biste dobili rezultat.
- Molarna masa solne kiseline je: 1,007 + 35,453 = 36,460 g / mol. Masa jednog mola HCl je 36,46 grama.
- Molarna masa glukoze je: 72,0642 + 12,084 + 95,9964 = 180,1446 g / mol. Masa jednog mola glukoze je 180,14 grama.
Savjeti
- Iako je većina relativnih atomskih masa poznata s točnošću od jednog dijela do deset tisuća (četiri decimale), u većini laboratorijskih radova molarne mase obično se navode na dvije decimale ili čak manje za posebno velike mase. Tako bi u laboratoriju molarna masa solne kiseline bila 36,46 g / mol, a glukoze 180,14 g / mol.
Potrebni materijali
- Knjiga kemije ili periodni sustav elemenata
- Kalkulator


