Autor:
Mike Robinson
Datum Stvaranja:
7 Rujan 2021
Datum Ažuriranja:
11 Svibanj 2024

Sadržaj
Atomski broj odgovara broju protona u jezgri pojedinog atoma elementa. Ova se vrijednost ne mijenja; stoga ga možete koristiti za otkrivanje drugih karakteristika izotopa, poput broja neutrona.
Koraci
Dio 1 od 2: Pronalaženje atomskog broja
Pronađite kopiju periodnog sustava. Kliknite ovdje ako ga nemate na raspolaganju. Svaki element ima svoj atomski broj; dakle, ne postoje prečaci za učenje sadržaja. Upotrijebite kopiju tablice ili je pokušajte upamtiti.
- Većina knjiga o kemiji ima tablicu otisnutu na stražnjoj korici.

Pronađite element koji proučavate u tablici. Većina tablica uključuje puno ime elemenata, kao i njihove simbole (Hg za živu, na primjer).Ako ne možete pronaći ono što tražite, povežite se na mrežu i pretražite pojmovima "kemijski simbol" i nazivom elementa.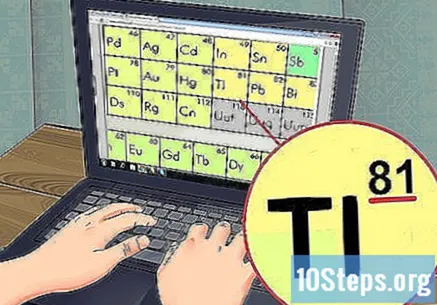
Pronađite atomski broj elementa. Obično je u gornjem lijevom ili desnom kutu kuće elementa, ali može doći i na drugim mjestima. Osim toga, to je uvijek cijela vrijednost.- Ako broj uključuje decimalnu točku, to vjerojatno označava atomsku masu.
Potvrdite podatke prema elementima u blizini. Periodni sustav organiziran je prema redoslijedu atomskih brojeva. Ako je na primjer vaš izotopski broj "33", element s lijeve strane bit će "32", a onaj s desne strane "34". U tom je slučaju to zato što gledate atomski broj.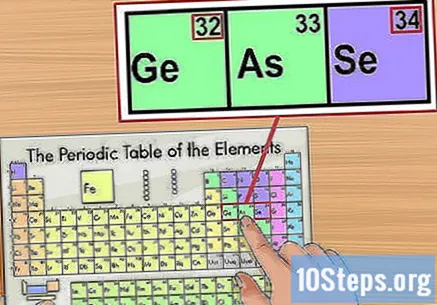
- Dolazi do skoka između elemenata "56" (barij) i "88" (radio). Izotopi koji odgovaraju ovom rasponu nalaze se u dva retka ispod tablice. Ovako su odvojeni samo da stol ne bude prevelik.
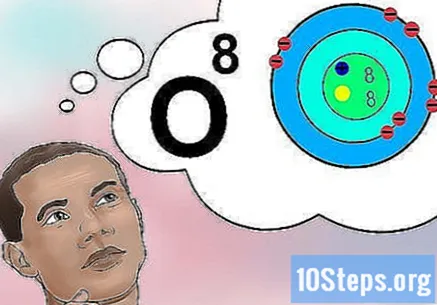
Shvatite što znači atomski broj. Atomski broj ima jednostavnu definiciju: količina protona u atomu elementa. Ova količina protona zauzvrat određuje ukupan električni naboj jezgre - što posljedično određuje koliko elektrona atom može napuniti. Budući da su elektroni odgovorni za gotovo sve kemijske interakcije, atomski broj neizravno utječe na fizikalna i kemijska svojstva elementa.- Drugim riječima, svaki atom s osam protona odgovara atomu kisika. Dva atoma kisika mogu imati različit broj neutrona ili (ako je jedan ion) ili elektrona, ali uvijek će imati po osam protona.
Dio 2 od 2: Otkrivanje važnijih informacija
Odrediti atomsku težinu. Obično dolazi pod imenom elementa u periodnom sustavu i ima dvije ili tri decimale. Atomska težina odgovara prosječnoj masi atoma elementa, predstavljajući kako se nalazi u prirodi. Mjeri se u "jedinicama atomske mase" ("u" ili "u.m.a").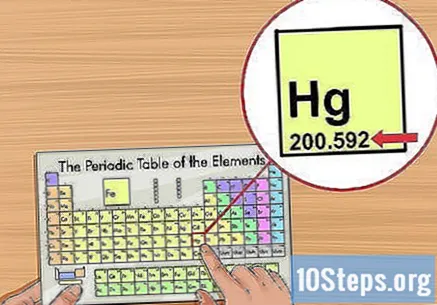
- Mnogi znanstvenici radije koriste izraz "atomska masa" umjesto težine.
Razumjeti atomsku masu. Koncept atomske mase vrlo je sličan konceptu težine. Razlika je u tome što težina ukazuje na prosječnu masu bilo kojeg atoma u elementu, a ne određenog atoma. Na primjer: gram željeza sadrži nekoliko atoma različitih masa; uteg pokazuje njihovu "relativnu masu". Ako proučavate jedan atom elementa, samo trebate znati njegovu specifičnu masu.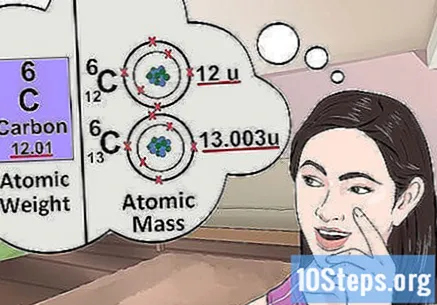
- Općenito, kemijski problemi koji uključuju samo atome već daju informaciju o atomskom masenom broju. Samo trebate razumjeti koncept da ne budete zatečeni kad vidite drugu vrijednost.
Zaokruži broj mase. Maseni broj odgovara ukupnoj količini protona i neutrona u atomu elementa. Nije ga teško izračunati: samo uzmite atomsku masu otisnutu na periodnom sustavu i zaokružite je na najbližu cijelu vrijednost.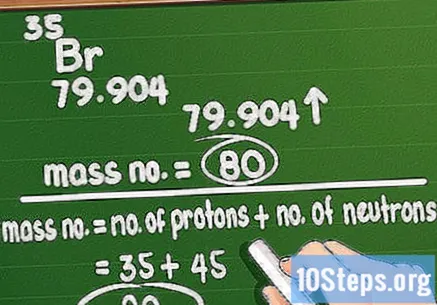
- To djeluje jer su količine neutrona i protona vrlo blizu 1 u.m.a., dok je količina elektrona vrlo blizu nuli. Atomska masa uključuje točne izračune za određivanje decimalne vrijednosti, ali jedini su važni podaci cijeli brojevi koji vam govore koliko protona i neutrona ima.
- Imajte na umu da ćete se, ako koristite atomsku masu, zabrljati s težinom određenog atoma u elementu. Na primjer, uzorak broma ima atomsku masu 79 ili 81.
Izračunaj broj neutrona. Sad već znate da je atomski broj jednak broju protona i da je maseni broj jednak zbroju broja protona i neutrona. Da biste odredili količinu neutrona u elementu, jednostavno oduzmite atomski broj od te ukupne mase. Neki primjeri:
- Atom helija (He) ima maseni broj 4 i atomski broj 2. Prema tome, 4 - 2 = 2 neutrona.
- Uzorak srebra (Ag) ima prosječni maseni broj 108 (prema periodnom sustavu) i atomski broj 47. U prosjeku svaki atom u uzorku ima 108 - 47 = 61 neutron.
Razumjeti izotope. Izotop je specifični oblik elementa koji sadrži brojne neutrone. Ako problem koji želite riješiti donosi nešto poput "bor-10" ili "B", to je zato što govorite o elementima bora s masenim brojem 10. Koristite ovu vrijednost, a ne "normalne" vrijednosti bora.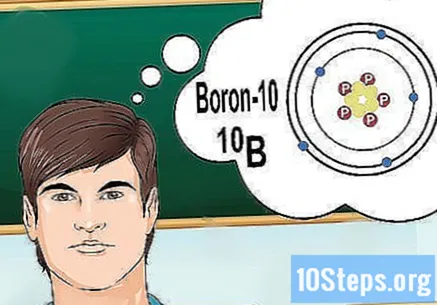
- Atomski broj izotopa nikada se ne mijenja. Svaki izotop elementa ima jednak broj protona.
Savjeti
- Atomska težina nekih težih elemenata dolazi u zagradama ili uglastim zagradama. To znači da je ova težina točna masa najstabilnijeg izotopa, a ne prosjek nekoliko izotopa. Konačno, to ne utječe na atomski broj elementa.