Sadržaj
Iako svi atomi istog elementa sadrže isti broj protona, broj neutrona može varirati. Znajući koliko neutrona pojedini atom može vam pomoći da odredite je li čestica pravilna u tom elementu ili izotopu, koji će imati više ili manje neutrona. Određivanje broja neutrona u atomu prilično je jednostavno i ne zahtijeva eksperiment. Da biste izračunali broj neutrona u običnom atomu ili izotopu, slijedite ove upute s periodičnom tablicom u ruci.
koraci
Metoda 1 od 2: Pronalaženje broja neutrala u zajedničkom atomu
Pronađite element u periodičnoj tablici. Za ovaj primjer, pogledajmo OS (Os) koji se nalazi u šestom redu, od vrha do dna.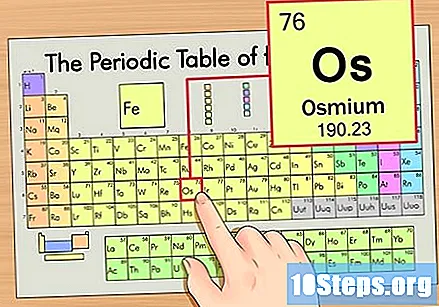
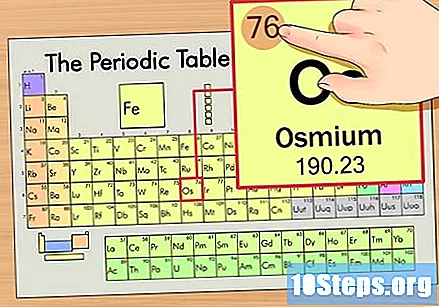
Pronađite atomski broj elementa. To je obično najvidljiviji broj određenog elementa i obično je iznad njegovog simbola (u tablici koju koristimo u stvari nije naveden drugi broj). Atomski broj je broj protona u jednom atomu tog elementa, Broj Os je 76, što znači da Osmij atom ima 76 protona.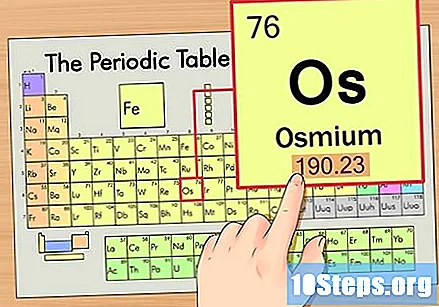
Pronađite atomsku težinu elementa. Taj se broj obično nalazi ispod atomskog simbola. Imajte na umu da se tablica u ovom primjeru temelji samo na atomskom broju i ne navodi atomsku masu. To neće uvijek biti slučaj. Osmij ima atomsku masu od 190,23.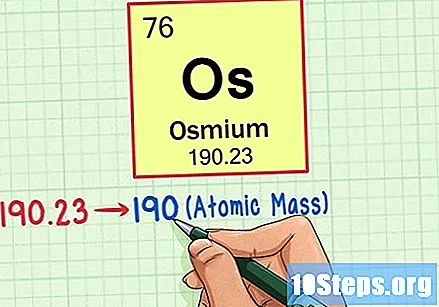
Zaokružite atomsku težinu na najbliži cijeli broj da biste pronašli atomsku masu. U našem primjeru 190,23 bi bilo zaokruženo na 190, što bi rezultiralo atomskom masom od 190 za Osmium.- Atomska masa je prosjek izotopa elementa. Stoga obično nije cijeli broj.
Oduzmi atomski broj od atomske mase. Budući da se velika većina mase atoma nalazi u njegovim protonovima i neutralima, oduzimanje broja protona (to jest, atomskog broja) od atomske mase dobit će vam broj izračunati neutrona u atomu. Broj nakon decimalne točke obično predstavlja vrlo malu masu elektrona u atomu. U našem primjeru to je: 190 (atomska masa) - 76 (broj protona) = 114 (broj neutrona).
Sjetite se formule. Da biste u budućnosti pronašli broj neutrona, samo koristite ovu formulu: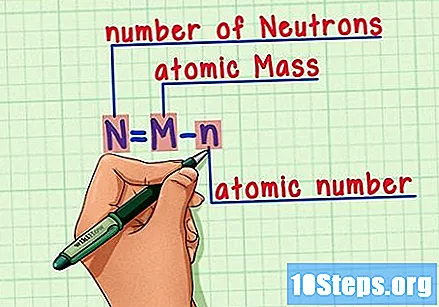
- N = M - n.
- N = broj od Neutrons.
- M = Matomsko pečenje.
- n = natomski humerus.
- N = M - n.
Metoda 2 od 2: Pronalaženje broja neutrona u izotopu
Pronađite element u periodičnoj tablici. Primjerice, upotrijebimo izotop ugljika-14. Kako je neizotopski oblik ugljika-14 jednostavno ugljik (C), pronađite ovaj element u periodnoj tablici (u drugom redu).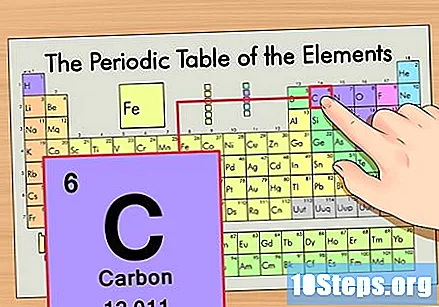
Pronađite atomski broj elementa. To je obično najvidljiviji broj određenog elementa i obično je iznad njegovog simbola (u tablici koju koristimo u stvari nije naveden drugi broj). Atomski broj je broj protona u jednom atomu tog elementa, C je broj 6, što znači da ugljikov atom ima 6 protona.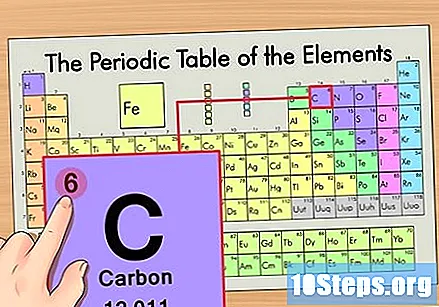
Pronađite atomsku masu. To je nevjerojatno lako s izotopima, kako su oni dobili ime po svojoj atomskoj masi. Ugljik-14 ima atomsku masu 14. Jednom kada pronađete atomsku masu izotopa, postupak pronalaska broja neutrona jednak je onome koji se koristi za obične atome.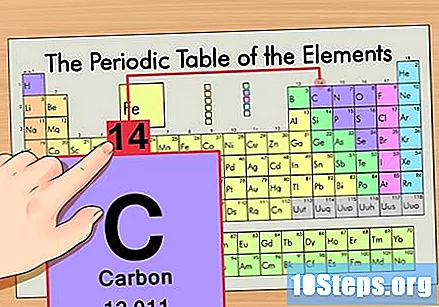
Oduzmi atomski broj od atomske mase. Budući da se velika većina mase atoma nalazi u njegovim protonovima i neutralima, oduzimanje broja protona (to jest, atomskog broja) od atomske mase dobit će vam broj izračunati neutrona u atomu. Broj nakon decimalne točke obično predstavlja vrlo malu masu elektrona u atomu. U našem primjeru to je: 14 (atomska masa) - 6 (broj protona) = 8 (broj neutrona).
Sjetite se formule. Da biste u budućnosti pronašli broj neutrona, samo koristite ovu formulu: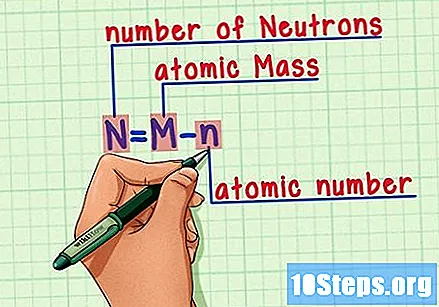
- N = M - n.
- N = broj od Neutrons.
- M = Matomsko pečenje.
- n = natomski humerus.
- N = M - n.
Savjet
- Osmij, čvrsti metal na sobnoj temperaturi, svoje je ime dobio od grčke riječi za "miris", "osme".
- Protoni i neutroni čine gotovo cjelokupnu težinu elemenata, dok elektroni i druge raznolike čestice predstavljaju zanemarivu masu (približavajući se nultoj masi). Kako je proton približno iste težine kao i neutralni, a atomski broj predstavlja broj protona, jednostavno možemo oduzeti broj protona od ukupne mase.
- Ako niste sigurni koji je broj koji se nalazi u periodičnoj tablici, samo zapamtite da se obično pravi oko atomskog broja (to jest, broja protona), koji započinje s 1 (Vodik) i ide gore s jednom jedinicom po slijeva udesno, završavajući sa 118 (Ununóctio). To je zato što broj protona u nekom atomu određuje kakav je taj atom, olakšavajući organizaciju elementarne karakteristike (na primjer, atom s dva protona uvijek će biti helij, baš kao što će drugi atom sa 79 protona uvijek biti Zlato).