Sadržaj
U kemiji Elektronegativnost to je mjera privlačnosti koju atom vrši na elektrone u vezi. Atom s velikom elektronegativnošću privlači elektrone s velikim intenzitetom, dok će atom s malom elektronegativnošću raditi s malim intenzitetom. Te se vrijednosti koriste za predviđanje ponašanja različitih atoma kada se međusobno povezuju, što ovu temu čini važnom vještinom osnovne kemije.
koraci
Metoda 1 od 3: Osnovni pojmovi elektronegativnosti
Shvatite da se kemijske veze događaju kada atomi dijele elektrone. Da biste razumjeli elektronegativnost, važno je prvo razumjeti što je "veza". Kaže se da svaka dva atoma u molekuli "povezana" u molekularnom dijagramu imaju međusobnu vezu. U osnovi, to znači da dijele skup od dva elektrona - svaki atom doprinosi atomu u vezi.
- Točni razlozi zašto atomi dijele elektrone i vezuju se zajedno ne odgovaraju fokusu ovog članka. Ako želite naučiti više, na internetu potražite osnovne pojmove kemijskih veza.
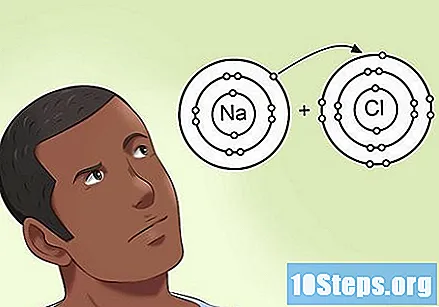
Shvatite kako elektronegativnost utječe na elektrone prisutne u vezi. Kad dva atoma dijele skup od dva elektrona u vezi, ne postoji uvijek jednaka podjela između dva. Kad jedan od njih ima veću elektronegativnost od atoma na koji je vezan, ona dva elektrona približava sebi. Atom s vrlo velikom elektronegativnošću može povući elektrone na svoju stranu u vezi, gotovo otkazujući dijeljenje s drugim.- Primjerice, u molekuli NaCl (natrijevog klorida) atom klora ima visoku elektronegativnost, a natrij malu elektronegativnost. Uskoro će se povući elektroni prema kloru i dalje od natrija.

Kao referencu koristite tablicu elektronegativnosti. Tabela elektronegativnosti prikazuje elemente raspoređene točno poput periodične tablice, ali sa svakim atomom označenom svojom elektronegativnošću. Oni se mogu naći u nekoliko udžbenika kemije, u tehničkim člancima i na internetu.- Evo izvrsne tablice elektronegativnosti. Imajte na umu da se koristi Paulingova skala elektronegativnosti, što je češće. Međutim, postoje i drugi načini mjerenja elektronegativnosti, od kojih će jedan biti prikazan u nastavku.
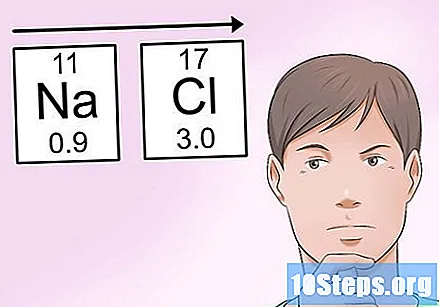
Zapamtite trendove elektronegativnosti da biste lako izračunali. Ako nemate pri ruci tablicu elektronegativnosti, još uvijek je moguće procijeniti tu vrijednost na temelju vašeg položaja u periodičnoj tablici. Kao opće pravilo:- Elektronegativnost atoma povećava kako se krećete prema pravo u periodičnoj tablici.
- Elektronegativnost atoma povećava kako se krećete gore u periodičnoj tablici.
- Dakle, atomi u gornjem desnom kutu imaju najveće vrijednosti elektronegativnosti, a oni u donjem lijevom kutu najnižu.
- Na primjer, u prethodnom primjeru NaCl možete odrediti da klor ima veću elektronegativnost od natrija jer je gotovo u najvišoj desnoj točki. S druge strane, natrij je daleko lijevo od stola, što ga čini jednim od najmanje vrijednih atoma.
Metoda 2 od 3: Pronalaženje veza s elektronegativnošću
Pronađite razliku elektronegativnosti između dva atoma. Kada su dva atoma povezana zajedno, razlika između njihovih vrijednosti elektronegativnosti puno otkriva o kvaliteti te veze. Oduzmite najmanju vrijednost od najveće da biste pronašli razliku.
- Na primjer, ako gledamo molekulu HF, oduzet ćemo vrijednost elektronegativnosti vodika (2.1) od vrijednosti fluora (4.0). 4,0 - 2,1 = 1,9.
Ako je razlika ispod 0,5, veza je kovalentna i nepolarna. Ovdje se elektroni dijele u gotovo jednakoj mjeri. Ove veze ne tvore molekule s velikim razlikama naboja na bilo kojem kraju. Polarne veze često je vrlo teško razbiti.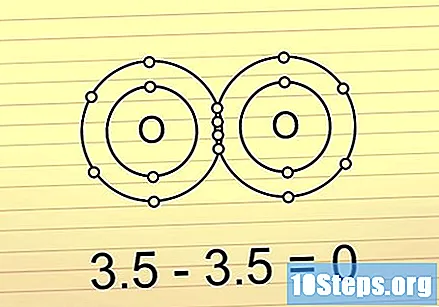
- Na primjer, molekula O2 predstavlja ovu vrstu veze. Budući da dvije molekule kisika imaju jednaku elektronegativnost, razlika između njih jednaka je 0.
Ako je razlika između 0,5 i 1,6, veza je kovalentna i polarna. Ove veze na jednom kraju drže više elektrona nego na drugom. To čini molekulu malo negativnijom na kraju s više elektrona i malo pozitivnijom na kraju bez njih. Neravnoteža naboja u tim vezama omogućava molekulama da sudjeluju u nekim specifičnim reakcijama.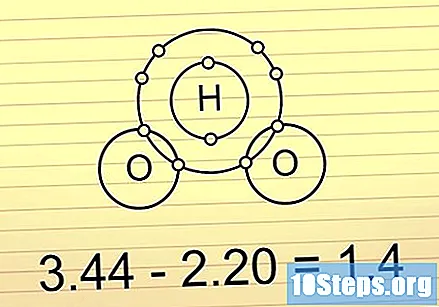
- Dobar primjer za to je molekula H2O (voda). O je elektronegativniji od dva H, tako da drži elektrone bliže i čitavu molekulu čini djelomično negativnom na O kraju, a djelomično pozitivnom na H krajevima.
Ako je razlika veća od 2, veza je ionska. U tim vezama elektroni su potpuno smješteni na jednom kraju. Najviše elektronegativnog atoma dobiva negativan naboj, a najmanje elektronegativni atom pozitivan naboj. Ova vrsta veze omogućuje atomima da reagiraju s drugim atomima ili, nadalje, da budu razdvojeni polarnim atomima.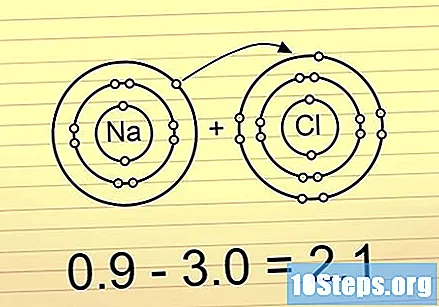
- Primjer za to je NaCl (natrijev klorid). Klor je toliko elektronegativan da povlači oba elektrona iz veze jedan prema drugom, ostavljajući natrij pozitivnim nabojem.
Ako je razlika između 1,6 i 2, potražite metal. Ako tamo metal prisutan u vezi, to ukazuje da jest ionski, Ako postoje drugi nemetali, veza je polarni kovalent.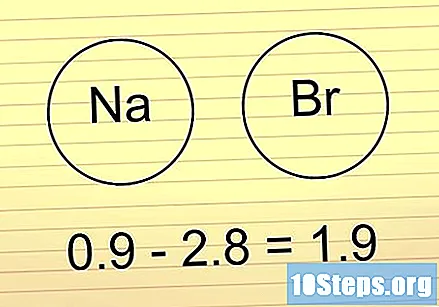
- Metali uključuju većinu atoma lijevo i u sredini periodičke tablice. Na ovoj se stranici nalazi tablica koja prikazuje koji su elementi metali.
- Naš prethodni primjer HF-a spada u tu skupinu. Budući da H i F nisu metali, veza će biti polarni kovalent.
Metoda 3 od 3: Otkrivanje elektronegativnosti Mulliken-a
Pronađite prvu energiju ionizacije vašeg atoma. Mulliken elektronegativnost sastoji se od metode mjerenja malo drugačiju od one utvrđene u Paulingovoj tablici gore. Da biste pronašli njegovu vrijednost za određeni atom, pronađite svoju prvu ionizacijsku energiju. Ovo je energija potrebna za ispuštanje atoma jednog elektrona.
- Ova se vrijednost vjerojatno može naći u kemijskim referentnim materijalima. Ova stranica ima dobru tablicu koju možete koristiti (pomaknite se prema dolje da biste je pronašli).
- Kao primjer, recimo da želite otkriti što je elektronegativnost litija (Li). U tablici na gornjoj stranici vidimo da je prva energija ionizacije jednaka 520 kJ / mol.
Otkrijte koji je afinitet atoma atoma. Ovo je mjerenje energije dobivene kada se atomu doda elektron da bi stvorio negativan ion. Ponovno, to je nešto što bi se trebalo naći u referentnim materijalima. Ova stranica ima resurse koji mogu biti korisni.
- Elektronski afinitet litija jednak je 60 kJ mol.
Riješite Mullikenovu jednadžbu elektronegativnosti. Kada se kJ / mol koristi kao energetska jedinica, Mullikenova jednadžba elektronegativnosti može se zapisati kao HRMulliken = (1,97 × 10) (Eja + Ei the) + 0,19, Umetnite poznate podatke u jednadžbu i pronađite vrijednost ENMulliken.
- U našem primjeru doći ćemo do sljedeće rezolucije:
- HRMulliken = (1,97 × 10) (Eja + Ei the) + 0,19
- HRMulliken = (1,97 × 10)(520 + 60) + 0,19
- HRMulliken = 1,143 + 0,19 = 1,333
- U našem primjeru doći ćemo do sljedeće rezolucije:
Savjet
- Pored vage Pauling i Mulliken, postoje i druge ljestvice elektronegativnosti, poput Allred-Rochow, Sanderson i Allen. Svaki od njih ima svoje jednadžbe za izračun elektronegativnosti (a neke od njih mogu biti i prilično složene).
- Elektronegativnost nema jedinicu mjere.